國家藥監局再出手,知名醫療器械企業被飛檢!
繼5月份國家藥品監督管理局對一批械企飛檢后,6月份,國家藥監局再出手,飛檢了6家械企,大有“每月一飛檢”的節奏。

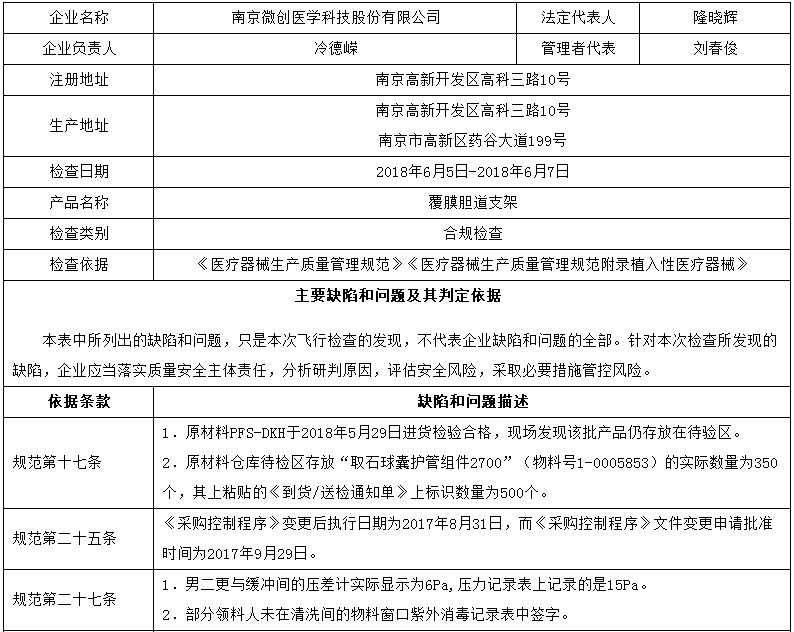
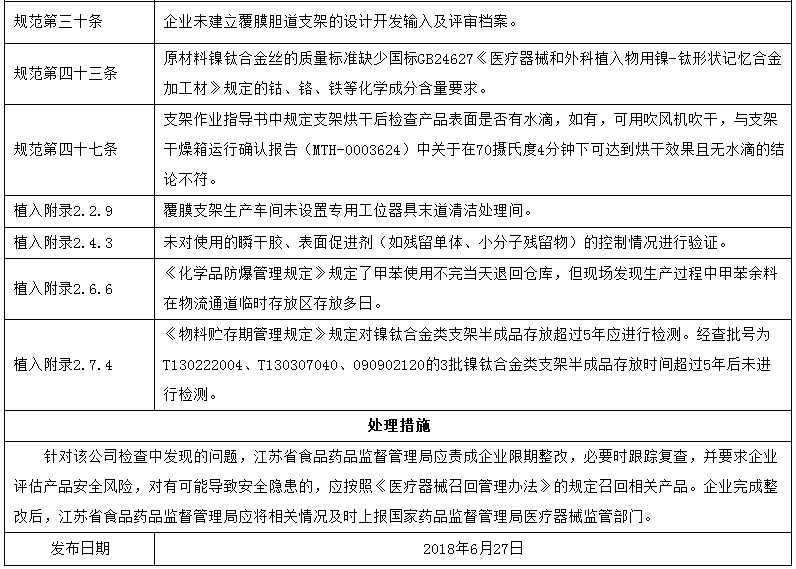
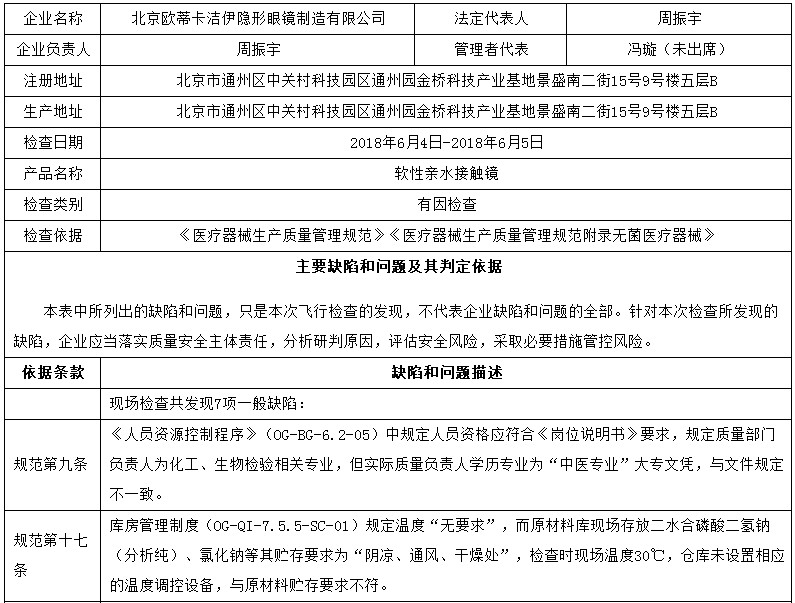

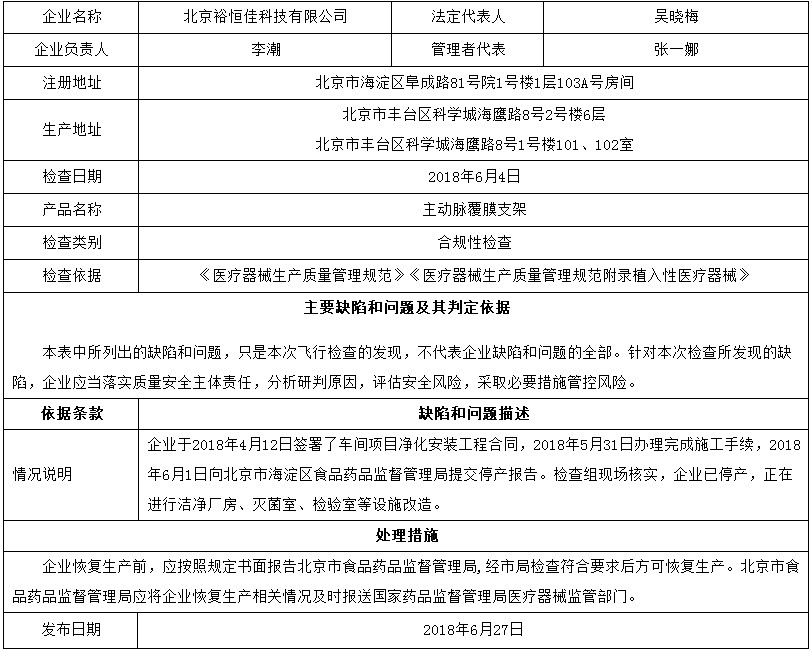
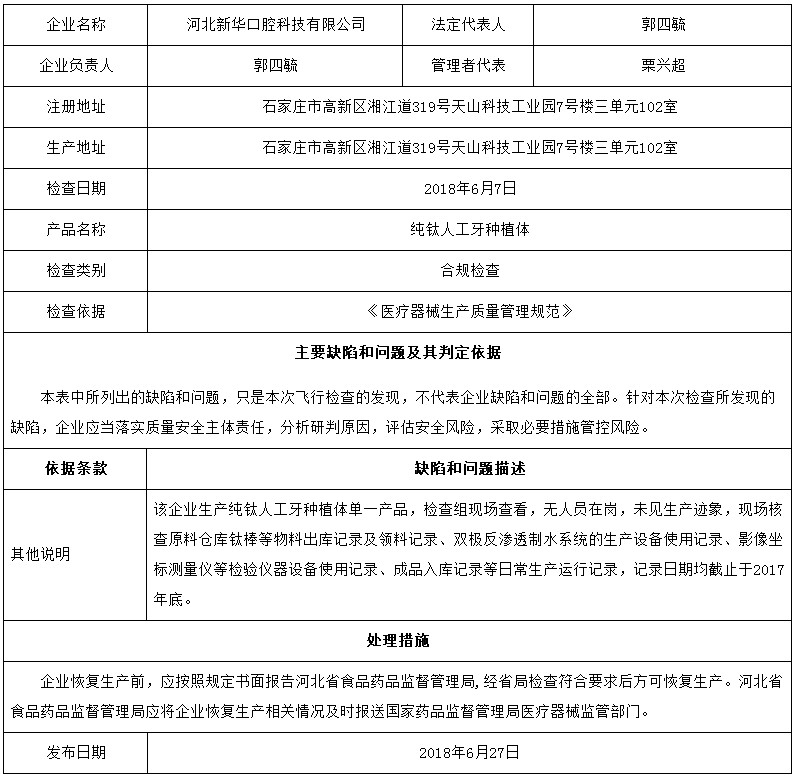
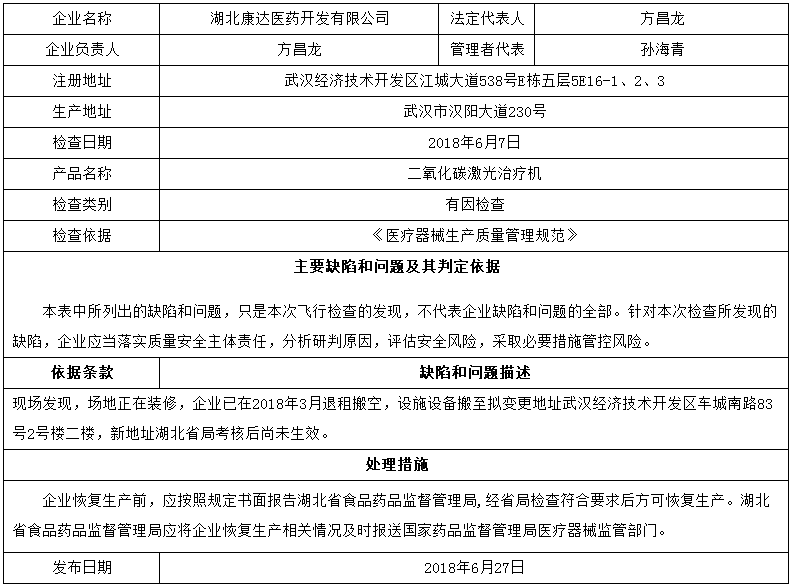
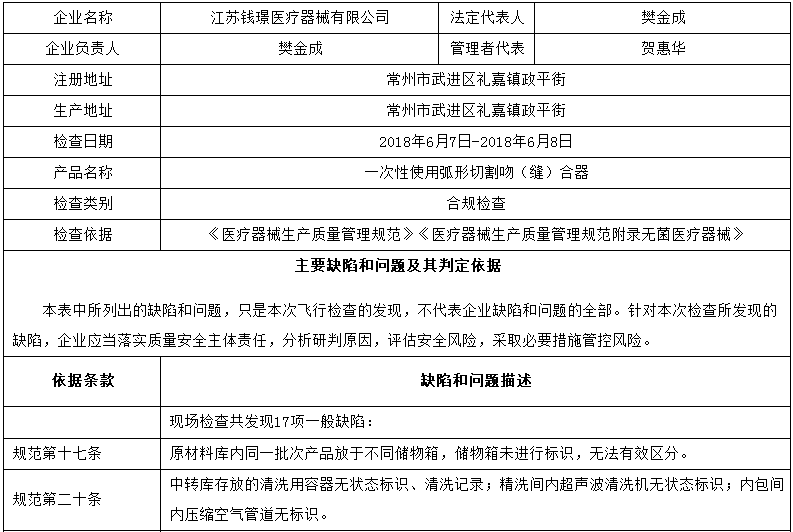
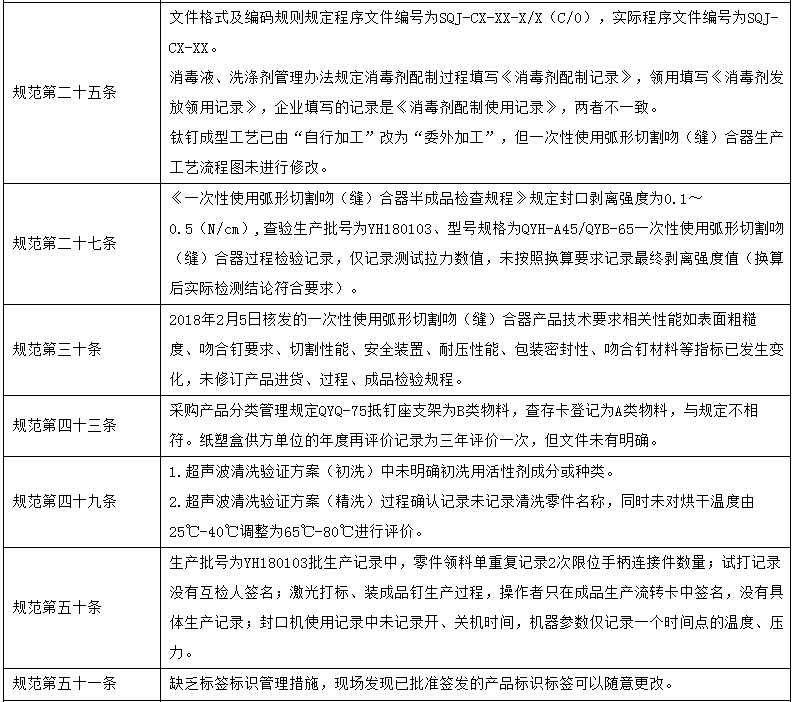

昨天,國家藥品監督管理局網站發布對6家醫療器械生產企業的飛檢通報,飛檢產品包括覆膜膽道支架、主動脈覆膜支架、純鈦人工牙種植體、二氧化碳激光治療機、一次性使用弧形切割吻(縫)合器等。

通報顯示,6家企業分別位于江蘇、湖北、河北、北京等省市,其中3家處于停產狀態,另外3家發現多處一般缺陷,被要求限期整改,這其中包括南京微創。
在醫療器械GMP全面實施的背景下,國家藥監局飛檢很頻繁,監管高壓之勢顯現。
以下為飛檢通報:
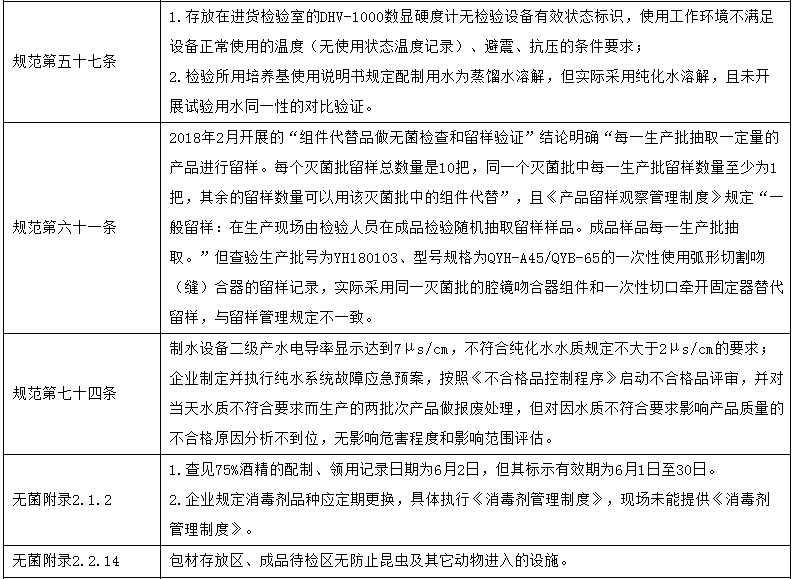
對南京微創醫學科技股份有限公司飛行檢查通報


對北京歐蒂卡潔伊隱形眼鏡制造有限公司飛行檢查通報


對北京裕恒佳科技有限公司飛行檢查通報

對河北新華口腔科技有限公司飛行檢查通報

對湖北康達醫藥開發有限公司飛行檢查通報

對江蘇錢璟醫療器械有限公司飛行檢查通報




-
 2025年廣東省關于部分醫用耗材掛網價格信息調整明細表(20250916批次)
2025年廣東省關于部分醫用耗材掛網價格信息調整明細表(20250916批次)
-
 2025年漳州市關于注射器全省性聯盟集中帶量采購符合報名要求的企業及產品名單
2025年漳州市關于注射器全省性聯盟集中帶量采購符合報名要求的企業及產品名單
-
 2025年漳州市關于一次性使用壓力延長管全省性聯盟集中帶量采購符合報名要求的企業及產品名單
2025年漳州市關于一次性使用壓力延長管全省性聯盟集中帶量采購符合報名要求的企業及產品名單
-
 2025年貴州省關于第一批一次性使用可收費集中帶量采購醫用耗材目錄
2025年貴州省關于第一批一次性使用可收費集中帶量采購醫用耗材目錄
-
 2025年青海省關于醫用耗材產品申報信息一覽表(第四十二批)2025.9.17
2025年青海省關于醫用耗材產品申報信息一覽表(第四十二批)2025.9.17
-
 2025年青海省關于口腔牙冠非競價產品申報信息一覽表(第十五批)
2025年青海省關于口腔牙冠非競價產品申報信息一覽表(第十五批)
-
 2025年青海省關于醫用耗材產品降價變更匯總表2025.9.16
2025年青海省關于醫用耗材產品降價變更匯總表2025.9.16
-
 2025年廣西壯族自治區關于中選產品掛網價格調整情況表(2025第二十一批—醫用耗材)
2025年廣西壯族自治區關于中選產品掛網價格調整情況表(2025第二十一批—醫用耗材)
-
 2025年淮南市關于一批普通醫用耗材聯動降價目錄
2025年淮南市關于一批普通醫用耗材聯動降價目錄




















